恒瑞医药
恒瑞医药是创新驱动转型的中国医药龙头。公司从传统仿制药起家,凭借突出的研发和销售能力,已在肿瘤、肌松麻醉、造影三大板块,成为国内绝对龙头。研发投入占收入比超过10%,已形成每年2-3个创新药上市的良性发展态势。公司正迅速从“仿制龙头”向“创新龙头”转型。
公司创新药今年将逐步迎来收获期。PD-1单抗上市申请获得CDE受理,并与国内其他3家申报的该品种一起纳入同一批拟优先审评,预计最快有望年底获批上市,峰值销售可达50-100亿人民币。自主研发麻醉新品种甲苯磺酸瑞马唑伦已于3月21日提交上市申请;新一代前列腺癌药物SHR3680于4月23日顺利进入Ⅲ期临床,二者研发进展超市场预期。
我们认为公司2017-19年净利润仍有望保持20%左右的增速。丰富的临床在研品种将为公司长远发展提供坚实动力。维持推荐评级,目标价98元对应2018/2019年市盈率71/59倍。风险包括新药研发进度不及预期,在售药品降价风险。
百济神州
百济神州是一家全球性生物医药公司。百济神州拥有超过300人构成的全球团队,其中包括约200位科学家和医学专家。公司目前拥有4个自主研发的靶向药物,其中BTK靶向药物BGB-3111与PD-1单抗BGB-A317均已进入Ⅲ期临阶段。此外公司PARP抑制剂BGB290与RAF二聚体BGB-283已进入Ⅰ期临床阶段。公司当前市值约110亿美元。百济神州PD-1单抗目前已有3项临床进入Ⅲ期临床阶段。公司目前总共有12项临床研究正在进行中,其中关于肝细胞癌、食管鳞状细胞癌、NSCLC的三项研究已进入Ⅲ期阶段。5项临床研究已进入2期,适应症包括霍奇金淋巴瘤、胃癌等。2017年7月,百济与美国制药巨头新基公司(Celgene)达成战略合作共同开发其PD-1单抗,授予Celgene实体瘤在亚洲之外(包括日本)的开发和商业化权利。同时百济接受新基在中国的运营团队,拥有新基在中国获批产品的独家授权。百济最快有望在今年提交上市申请,2019年有望获批上市。

优卡迪
优卡迪(Unicar-Therapy)是全国资深的CAR-T细胞技术和产品研发的生物技术公司。自2015年由在美国有23年细胞免疫治疗经验的海归博士俞磊建立以来,已与全国各地多家优质三甲医院血液科建立临床合作关系,在苏医附一院、陕西省人民医院、中南大学湘雅三院和哈尔滨医科大学等多临床中心对超过200多例复发难治性白血病、复发难治性淋巴瘤和复发难治性多发性骨髓瘤的CAR-T疗法进行了多层次的临床研究。
参考观研天下发布《2018年中国生物医药行业分析报告-市场运营态势与投资前景预测》
研发产品线丰富,血液瘤到实体瘤多病种覆盖。公司研发了全球独特的可以降低CRS风险的sCAR-T技术(safeCAR-T),并开发了丰富的覆盖了最常见的血液肿瘤的sCAR-T产品管线,针对CAR-T疗法在急性难治复发性白血病、复发难治(非)霍奇金淋巴瘤和进展性多发性骨髓瘤的多个产品已经进入临床试验阶段,并显示出预期的临床结果;优卡迪公司在大量的CAR-T临床治疗血液肿瘤的科研基础上,同时也针对多种实体瘤进行研发,主要包括脑胶质瘤、前列腺癌、胰腺癌等。
复宏汉霖
复宏汉霖为复星医药与美国科学家团队于2009年合资组建,专注于生物类似药、生物改良药以及单抗创新的生物科技公司。公司在研产品聚焦肿瘤与自身免疫性疾病。截至目前,公司已完成11个产品、16项适应证IND申报。虽然公司在肿瘤免疫原研药上,还不处于本土公司的第一梯队,但其生物类似药有望走向欧美市场。到2023年将有超过1150亿美元(按2022年销售额计算)的生物药专利到期。出于控制医疗成本的目的,美欧监管部门都在大力提倡生物类似药的审批,此前困扰生物类似药销售的互换性监管问题等都有望在未来一到两年内解决。
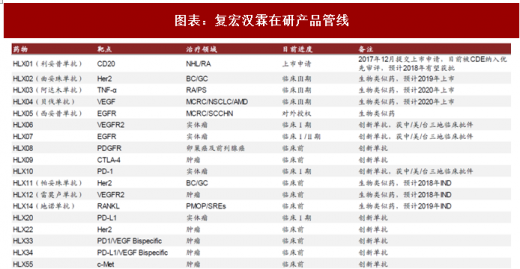
公司研发管线亮点包括:1)公司CD20利妥昔单抗的生物类似药HLX01,2017年12月提交上市申请,目前被CDE纳入优先审评,预计2018年有望获批,进度为国内第一。CD20原研药物利妥昔单抗(美罗华)是罗氏销售多年的重磅产品,主要用于CD20阳性的弥漫大细胞淋巴瘤等,2017年全球销售额为75亿美元。美罗华2017年在国内样本医院销售额已超过10亿人民币。2)公司曲妥珠单抗的生物类似药HLX02,目前均处于Ⅲ期临床试验中,预计2019年上市。3)阿达木单抗生物类似药HLX03与贝伐单抗生物类似药HLX04目前均处于Ⅲ期临床试验中,预计2020年上市。此外,复宏汉霖的PD-1单抗HLX10于2017年陆续获中/美/台三地临床批件,正开展国际多中心临床试验;PD-L1单抗HLX20也于2017年12月获批临床。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。








